
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Тема 7. Первое начало термодинамики. Внутренняя энергия. Работа. Применение первого начала термодинамики к изопроцессам.
|
|
Внутренней энергией газа U называется сумма кинетической энергии хаотического (теплового) движения всех молекул газа и энергии взаимодействия молекул газа между собой. Для идеального газа внутренняя энергия – это только кинетическая энергия всех молекул газа.
Внутренняя энергия идеального газа определяется числом степеней свободы его молекул и температурой газа.
Числом степеней свободы i механической системы называется количество независимых величин, с помощью которых может быть однозначно задано положение системы в пространстве.
Согласно закону о равнораспределении энергии по степеням свободы молекул для термодинамической системы, находящейся в равновесии, на каждую поступательную и вращательную степени свободы приходится в среднем кинетическая энергия, равная 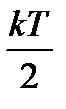 , а на каждую колебательную степень свободы – в среднем энергия, равная kT. Колебательная степень «обладает» вдвое большей энергией потому, что на нее приходится не только кинетическая энергия (как в случае поступательного и вращательного движений), но и потенциальная, причем средние значения кинетической и потенциальной энергий одинаковы.
, а на каждую колебательную степень свободы – в среднем энергия, равная kT. Колебательная степень «обладает» вдвое большей энергией потому, что на нее приходится не только кинетическая энергия (как в случае поступательного и вращательного движений), но и потенциальная, причем средние значения кинетической и потенциальной энергий одинаковы.
Таким образом, средняя кинетическая энергия молекулы:
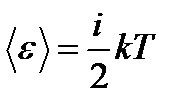 ,
,
где i – сумма числа поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекулы:
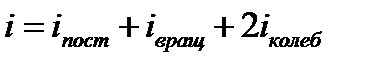 .
.
Внутренняя энергия N молекул идеального газа:
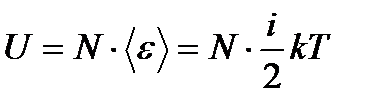
Так как число молекул газа 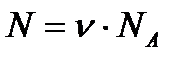 (NА – число Авогадро), где
(NА – число Авогадро), где 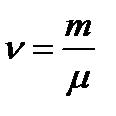 ,
,
то, с учетом соотношения 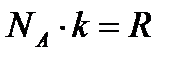 , получим:
, получим:
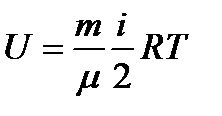 .
.
Изменение внутренней энергии ∆ U при изменении температуры от Т 1до Т 2:
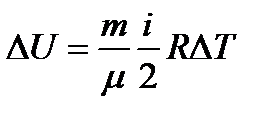 , где
, где 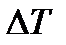 = Т 2 – Т 1 .
= Т 2 – Т 1 .
Внутреннюю энергию газа можно увеличить за счет сообщения ему некоторого количества теплоты 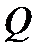 , которое может быть израсходовано также и на совершение механической работы А по расширению газа. При этом соблюдается закон сохранения и превращения энергии. Применительно к термодинамическим процессам это и есть первое начало термодинамики: количество теплоты
, которое может быть израсходовано также и на совершение механической работы А по расширению газа. При этом соблюдается закон сохранения и превращения энергии. Применительно к термодинамическим процессам это и есть первое начало термодинамики: количество теплоты 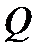 , сообщаемое термодинамической системе, расходуется на изменение ее внутренней энергии ∆ U и на совершение механической работы А против внешних сил:
, сообщаемое термодинамической системе, расходуется на изменение ее внутренней энергии ∆ U и на совершение механической работы А против внешних сил:
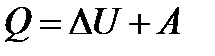 .
.
Работа А, совершаемая газом при изменении его объема от V 1 до V 2:
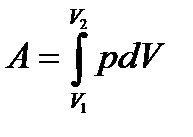 ,
,
где 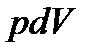 – элементарная работа при изменении объема газа на
– элементарная работа при изменении объема газа на 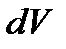 .
.
|
|